 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
在25.00mLBaCla试液中加入40.00mL 0.1020mol·L-1AgNO3标准溶液,过量的AgNO3标准
溶液在返滴定中用去15.00mL 0.09800mol·L-1NH4SCN标准溶液。试求25.00ml试液中含有BaCl2的质量,已知M(BaCl2)=208.24g·mol-1。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在25.00mLBaCla试液中加入40.00mL 0.10…”相关的问题
更多“在25.00mLBaCla试液中加入40.00mL 0.10…”相关的问题
A.在稀的和热的溶液中进行沉淀
B.在热的和浓的溶液中进行沉淀
C.在不断搅拌下向试液逐滴加入沉淀剂
D.沉淀剂一次加入试液中
E.正确生成的沉淀进行水浴加热或存放
取含Bi3+,Pb2+,Cd2+的试液25.00cm3,以二甲酚橙为指示剂,在pH=1.0时用0.02015mol·dm-3的EDTA滴定,用去20.28cm3。调节pH=5.5,用EDTA继续滴定,又用去30.16cm3;再加入邻二氮菲,用0.02002mol·dm-3Pb2+标准溶液滴定,用去10.15cm3。计算溶液中Bi3+,Pb2+和Cd2+的浓度。
用氟离子选择电极作负极:SCE作正极,取不同体积的含F-标准溶液
(CF-=2.0X10-4mol·L-1),加入一定的TISAB,稀释至100mL,进行电位法测定,测得数据如下:
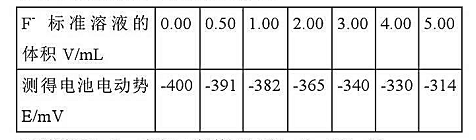
取试液20mL,在相同条件下测定,E=-359mV.
(a)绘制E一–lgCrF-工作曲线.
(b)计算试液中F-的浓度.
MnO4-及MnO42-岐化生成的MnO4-和MnO2全部还原为Mn2+,剩余的Fe2+溶液用上述KMnO4标准溶液滴定至终点,消耗24.00mL.计算试液中HCOOH和HOAc的浓度各为多少?