 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
向四个体积相同的密闭容器中分别充入一定量的SO2和O2,开始反应时,按反应速率由大到小的排列顺序正确的是()
A.甲、乙、丙、丁
B.乙、甲、丙、丁
C.乙、甲、丁、丙
D.丁、丙、乙、甲
 答案
答案
C、乙、甲、丁、丙
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.甲、乙、丙、丁
B.乙、甲、丙、丁
C.乙、甲、丁、丙
D.丁、丙、乙、甲
 答案
答案
C、乙、甲、丁、丙
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“向四个体积相同的密闭容器中分别充入一定量的SO2和O2,开始…”相关的问题
更多“向四个体积相同的密闭容器中分别充入一定量的SO2和O2,开始…”相关的问题
A.甲、乙、丙、丁
B.乙、甲、丁、丙
C.乙、甲、丙、丁
D.丁、丙、乙、甲
A.SO2和SO3的物质的量一定相等
B.NO2和SO3的物质的量一定相等
C.反应混合物的总物质的量一定等于反应开始时NO2和SO2的总物质的量
D.SO2、NO2、NO、SO3的物质的量一定相等
500℃时,可逆反应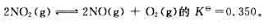 如果将一定量NO2(g)充入一不含任何气体的密闭容器中,平衡时测得NO(g)的分压34.4kPa.则NO2(g)的初始分压为().O2(g)的平衡分压为(),NO(g)的平衡分压为,NO(g)的平衡解离度为()。
如果将一定量NO2(g)充入一不含任何气体的密闭容器中,平衡时测得NO(g)的分压34.4kPa.则NO2(g)的初始分压为().O2(g)的平衡分压为(),NO(g)的平衡分压为,NO(g)的平衡解离度为()。
A.1.6mol
B.1.2mol
C.大于1.6mol
D.小于1.2mol
A.升高温度,K增大
B.减小压强,n(CO2)增加
C.更换高效催化剂,α(CO)增大
D.充入一定量的氮气,n(H2)不变
A.增加焦炭的量
B.保持体积不变,充入H2O气使体系的压强增大
C.将容器的体积增大一倍
D.将容器的体积缩小为一半
A.不变
B.增大
C.减小
D.无法判断
A.容器中三氧化硫体积保持不变
B.容器中混合物的压强保持不变
C.混合物的总的物质的量保持不变
D.容器中SO2、O2与SO3的物质的量之比为2︰1︰2
A.当v(CO)(正)=v(H2)(正),时,反应达到平衡状态
B.其他条件不变,适当增加C(s)的质量会使平衡正向移动
C.保持容器体积不变,充入少量He使体系压强增大,反应速率一定增大
D.其他条件不变,仅将容器的体积缩小一半,再次达到平衡时,H20(g)的平衡浓度可能是原来的2.1倍
氮化镓(GaN)是第三代半导体材料,具有热导率高、化学稳定性好等性质,在光电领域和高频微波器件应用等方面有广阔的前景。
(1)传统的氮化镓制各方法是采用GaC13与NH3在一定条件下反应。NH3的电子式为()。
(2)Johnson等人首次在1100℃下用液态镓与氨气制得氮化镓固体,该可逆反应每生成1molH2放出10.3kJ热量。其热化学方程式为()。
(3)在恒容密闭容器中,加入一定量的液态镓与氨气发生上述反应,测得反应平衡体系中NH3的体积分数与压强(p)、温度(T)的关系如图所示。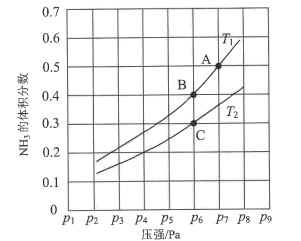 ①下列说法正确的是()(填标号)。
①下列说法正确的是()(填标号)。
a.温度:T1>T2
b.当百分含量ω(NH3)=ω(H2)时,说明该反应处于化学平衡状态
c.A点的反应速率小于C点的反应速率
d.温度恒定为T2,达平衡后再充入氦气(氦气不参与反应),NH3的转化率不变
②既能提高反应速率又能使平衡正向移动的措施有()(写出一条即可)。
③气体分压(p分)=气体总压(p总)×体积分数,用平衡分压代替物质的量浓度也可以表示平衡常数(记作Kp)。在T2时,用含p6的计算式表示C点的()。
(4)如图可表示氮化镓与铜组装成的人工光合系统的工作原理。H+向()(填“左”或“右”)池移动;铜电极上发生反应的电极反应式为()。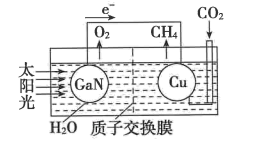
A.2v(NH3) = v(CO2)
B.密闭容器中混合气体的密度不变
C.密闭容器中混合气体的平均摩尔质量不变
D.密闭容器中氨气的体积分数不变