 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
KF晶体属于NaCl构型,试利用Born-Lande公式计算KF晶体的晶格能.已知从Born-Lande循环求得的晶格能为802.5kJ·mol-1,比较实验值和理论值的符合程度如何.
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“KF晶体属于NaCl构型,试利用Born-Lande公式计算…”相关的问题
更多“KF晶体属于NaCl构型,试利用Born-Lande公式计算…”相关的问题
已知NaCl的晶体结构如图C.17.1所示,它属于立方晶系,Oh点群。晶胞参数=564.0pm。
(I)写出通过晶胞中心的点对称元素。
(2)根据Na+和Cl-的离子半径值,了解在这结构中负离子是否接触?这种结构的稳定性如何?
(3)试计算NaCl晶体的密度D。
(4)将图C.17.1晶胞中顶角上的Na+和中心的Cl-除去,将Na+换成Nb2+,Cl-换得O2-即得NbO晶胞,试画出NbO的晶胞和其中原子簇的结构;已知晶跑参数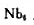 =421pm,计算晶体的密度i写出通过晶胞中心点的点对称元素和点群(Nb的相对原子质量为92.91);计算Nb2+的离子半径。
=421pm,计算晶体的密度i写出通过晶胞中心点的点对称元素和点群(Nb的相对原子质量为92.91);计算Nb2+的离子半径。
(5)将图C.17.1晶胞中面心和体心的原子除去,顶角上的Na+换成U6+,棱上的Cl-换成O2-,得UO3的晶体结构,立方晶胞参数a=415.6pm。试画出UO3晶胞的结构;写出通过晶胞中心点的点对称元素和点群;计算晶体的密度,计算U6+的离子半径(U的相对原子质量为238.0);画出由处在12条棱上的02-组成的立方八面体的图形;计算该多面体的自由孔径。
试根据价层电子对互斥理论推出下列情况下ABn型分子的几何构型:
(1)中心原子A的价层电子对数为6,配体B的个数n=4;
(2)中心原子A的价层电子对数为5,配体B的个数n=2。
并利用得出的结论判断下列分子或离子的几何构型:
(3)I3-;(4)XeF2;(5)XeF4;(6)ICl4-。
A.配合物的Kf>>沉淀的Ksp
B.配合物的Kf较小,沉淀的Ksp较大
C.配合物的Kf较大,沉淀的Ksp较大
D.配合物的Kf较大,沉淀的Ksp较小