题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
原电池中进行的电化学反应为热力学()过程,在原电池中,正极即是()极,负极即是()极。
原电池中进行的电化学反应为热力学()过程,在原电池中,正极即是()极,负极即是()极。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“原电池中进行的电化学反应为热力学()过程,在原电池中,正极即…”相关的问题
更多“原电池中进行的电化学反应为热力学()过程,在原电池中,正极即…”相关的问题
在不耐蚀的金属中加入()稳定性高的合金元素,提高了金属的耐蚀性。
A.电化学
B.热力学
C.耐湿热
D.耐大气
现有KNO3和NaNO2的混合样品5.000g,制备成500.0mL的溶液,移液25.00mL,用浓度为0.1200mol·L-1的Ce4+标准溶液50.00mL在强酸中氧化,过量的Ce4+用浓度为0.02500mol·L-1的Fe2+标准溶液滴定,用去Fe2+溶液28.40mL,相应的反应如下:
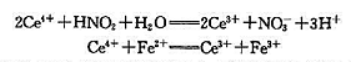
(1)若将第一个反应式作为原电池的电池反应写出该原电池的电极反应并计算该电池反应的ΔrGmθ[已知ϕθ(Ce4++/Ce3+)=1.44V,ϕθ(NO3-/NO2-)=0.934V]
(2)计算试样中NaNO2的质量分数w.[已知M(NaNO2)=69.00g.mol-1]
(3)计算第一步的标准平衡常数Kθ.
解题思路:注意原电池的写法.此题依然是考查电化与热力学、化学平衢间的计算.
A.结晶是固体物质以晶体形态从溶液中析出的过程
B.沉淀是固体物质以无定形态从溶液中析出的过程
C.结晶是一个热力学不稳定的多相多组分传质传热过程
D.沉淀是同类分子或离子进行规则排列的结果
A.第二类永动机是不可能制造出来的
B.把热从低温物体传到高温物体,不引起其它变化是不可能的
C.一切实际过程都是热力学不可逆过程
D.功可以全部转化为热,但热一定不能全部转化为功
E.孤立系统中,自发过程是向着体系熵增大的方向进行
298K,标准状态下,利用热力学数据求算下列反应的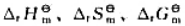 ,并根据求得数据说明,此反应在净化汽车尾气中的NO和CO时,在理论上的可能性。
,并根据求得数据说明,此反应在净化汽车尾气中的NO和CO时,在理论上的可能性。