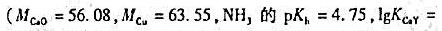题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
某试液中Cu2+和Ag+浓度均为2.0×10-2mol·dm-3,以0.40 mol·dm-3
氨性缓冲溶液控制pH=10.0,然后用2.0×10-2mol·dm-3EDTA滴定其中Cu2+,计算lg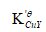 ,若以紫脲酸氨为指示剂(pH=10时,pCut=13.8),计算终点误差。
,若以紫脲酸氨为指示剂(pH=10时,pCut=13.8),计算终点误差。
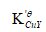 ,若以紫脲酸氨为指示剂(pH=10时,pCut=13.8),计算终点误差。
,若以紫脲酸氨为指示剂(pH=10时,pCut=13.8),计算终点误差。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
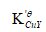 ,若以紫脲酸氨为指示剂(pH=10时,pCut=13.8),计算终点误差。
,若以紫脲酸氨为指示剂(pH=10时,pCut=13.8),计算终点误差。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某试液中Cu2+和Ag+浓度均为2.0×10-2mol·dm…”相关的问题
更多“某试液中Cu2+和Ag+浓度均为2.0×10-2mol·dm…”相关的问题
电解Cu2+和Sn2+的混合酸性溶液,Cu2+和Sn2+的浓度均为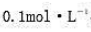 ,以铂为电极进行电解。
,以铂为电极进行电解。
(1)在阴极上何种离子先析出?
(2)若要使两种金属离子完全分开,阴极电位应控制多少?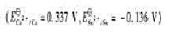
A.φCu2+/Cu<φ()<φAg+/Ag
B.φCu2+/Cu<φ(-)<φAg+/Ag
C.φ()>φAg+/Ag
D.φ(-)=φH+/H2
l3+,Zn2+,Fe3+,cu2+。
物)5.00ml,加水稀释至刻度,摇匀,作为对照品溶液。精密量取酊剂溶液7.50ml,置100ml量瓶中,加入正丙醇5.00ml,加水稀释至刻度,摇匀,作为供试液。分别取对照品溶液和供试液1μl注入气相色谱仪,对照品分析时乙醇和丙醇的峰面积分别为1539μV·s和1957μV·s,供试液分析时乙醇和丙醇的峰面积分别为1637μV·s和2012μV·s。计算酊剂中乙醇浓度。
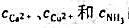 的浓度各为多少?(2)能否在Cu2+存在下,用EDTA准确滴定Ca2+?
的浓度各为多少?(2)能否在Cu2+存在下,用EDTA准确滴定Ca2+?