 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
设C(s)+CO2(g) = 2CO(g) ΔH>0的反应速率为v1,N2(g)+3H2(g) = 2NH3(g) ΔH<0的反应速率为v2,对于这两个反应,当温度升高时,v1和v2的变化情况为()
A.同时增大
B.同时减小
C.v1增大,v2减小
D.v1减小,v2增大
 答案
答案
A、同时增大
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.同时增大
B.同时减小
C.v1增大,v2减小
D.v1减小,v2增大
 答案
答案
A、同时增大
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“设C(s)+CO2(g) = 2CO(g) ΔH>0的反应速…”相关的问题
更多“设C(s)+CO2(g) = 2CO(g) ΔH>0的反应速…”相关的问题
A.①②③④
B.②③④⑤
C.①②③
D.②③④
A.5
B.4
C.3
D.2
已知下列反应在298.15K的平衡常数:
(1)SnO2(s)+2H2(g) 2H2O(g)+Sn(s)
2H2O(g)+Sn(s)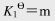
(2)H2O(g)+CO(g) H2(g)+CO2(g);
H2(g)+CO2(g);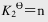
计算反应2CO(g)+SnO2(s) Sn(s)+2CO2(g)在298.15K时的平衡常数KΘ3。
Sn(s)+2CO2(g)在298.15K时的平衡常数KΘ3。
A.①②③④
B.①③④
C.①②
D.①③
A.在平衡混合物中 c(CO):c(CO2) = 2:1
B.碳和二氧化碳不再化合,一氧化碳不再分解
C.单位时间内,若消耗 n mol二氧化碳,同时消耗 n mol碳
D.平衡时,若条件不变,则二氧化碳和一氧化碳的浓度不变
对于生命起源问题,有人提出最初植物或动物的复杂分子是由简单分子自动形成的。例如,尿素(NH2CONH2)的生成可用反应方程式表示如下: CO2(g)+2NH3(g)→(NH2)2CO(s)+H2O(1) (1)计算上述反应在298K时的标准摩尔自由能变,说明反应在298K、标准状态下能否自发进行。 (2)在标准状态下,最高温度为何值时,反应就不再自发进行了? CO2(g)+2NH3(g)→(NH2)2CO(s)+H2O(1)
在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
问题一、已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJ/mol2C(s)+O2(g)=2CO(g)△H=-221.0kJ/molC(s)+O2(g)=CO2(g)△H=-393.5kJ/mol尾气转化的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=()
问题二、某研究性学习小组在技术人员的指导下,按以下流程探究某种催化剂在不同空燃比(空气与燃油气的质量比)条件下对汽车尾气的催化效果。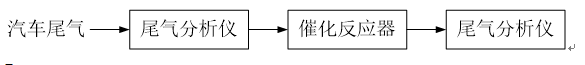
①实验过程中除空燃比不同外,其他条件:汽车尾气的流速、()等必须相同。
②在一定条件下,测得尾气中的主要污染物的转化率与空燃比的关系如右图所示。空燃比约为()时,催化剂对汽车尾气的催化效果最好。
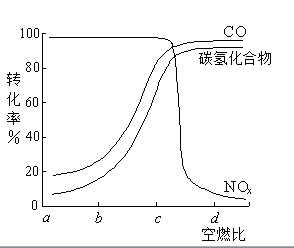
问题三、CO分析仪以燃料电池为工作原理,其装置如下图,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动。以下说法错误的选项是()。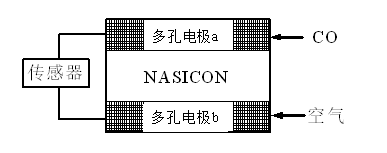
A负极的电极反应式为:CO+O2—―2e-=CO2
B工作时电极b作正极,O2-由电极a流向电极b
C工作时电子由电极a通过传感器流向电极b
D传感器中通过的电流越大,尾气中CO的含量越高
A.反应前2 min的平均速率v(SO2)=0.1a mol·L-1·min-1
B.当混合气体的物质的量不再改变时,反应达到平衡状态
C.平衡后保持其他条件不变,从容器中分离出部分硫,平衡向正反应方向移动
D.平衡后保持其他条件不变,升高温度和加入催化剂,SO2的转化率均增大
CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=+247kJ/mol
C—H键的键能约为413kJ/mol,O—H键的键能约为463kJ/mol,H—H键的键能约为436kJ/mol,则CO2中C=O键的键能约为()。
A.797.5kJ/mol
B.900.5kJ/mol
C.962.5kJ/mol
D.1595kJ/mol
A.升高温度可使该反应的逆反应速率降低
B.达到化学平衡时,化学反应已经停止
C.v正(NO)=v正(CO2)时,说明达到了化学平衡
D.单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡
压力变化不会使下列化学反应的平衡移动的是()。
A.H2(g)+I2(g)→2HI(g)
B.3H2(g)+N2(g)→2NH3(g)
C.2S02(g)+02(g)→2S03(g)
D.C(s)+C02(g)→2CO(g)