 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
试用热力学数据表计算823K下以下反应的及:(1)CoO(s)+H2(g)=Co(s)+H2O(g)(2)CoO(s)+CO
试用热力学数据表计算823K下以下反应的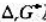 及
及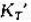 :
:
(1)CoO(s)+H2(g)=Co(s)+H2O(g)
(2)CoO(s)+CO(g)=Co(s)+CO2(g)
并讨论H2和CO还原CoO为Co的可能性,你以为哪种方法更好一些?为什么?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
试用热力学数据表计算823K下以下反应的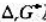 及
及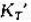 :
:
(1)CoO(s)+H2(g)=Co(s)+H2O(g)
(2)CoO(s)+CO(g)=Co(s)+CO2(g)
并讨论H2和CO还原CoO为Co的可能性,你以为哪种方法更好一些?为什么?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“试用热力学数据表计算823K下以下反应的及:(1)CoO(s…”相关的问题
更多“试用热力学数据表计算823K下以下反应的及:(1)CoO(s…”相关的问题
查热力学数据表,计算反应

800K时的 。进一步计算反应混合物为下列(1),(2)两种组成时的
。进一步计算反应混合物为下列(1),(2)两种组成时的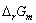 ,从而判断该两种组成时反应进行的方向。
,从而判断该两种组成时反应进行的方向。

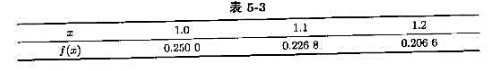
设已知函数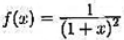 的数据表(表5-3),试用三点公式计算f'(x)在x=1.0,1.1,1.2处的近似值,并估计误差。
的数据表(表5-3),试用三点公式计算f'(x)在x=1.0,1.1,1.2处的近似值,并估计误差。
已知下列100kPa,298K时的热力学数据:
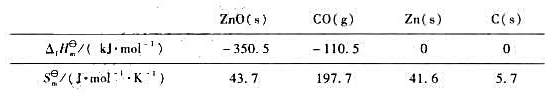
(1)试通过热力学计算,说明下面反应298K时的进行方向:
ZnO(s)+C(s)=Zn(s)+CO(g)
(2)求算上面反应自发正向进行的最低温度。
现有KNO3和NaNO2的混合样品5.000g,制备成500.0mL的溶液,移液25.00mL,用浓度为0.1200mol·L-1的Ce4+标准溶液50.00mL在强酸中氧化,过量的Ce4+用浓度为0.02500mol·L-1的Fe2+标准溶液滴定,用去Fe2+溶液28.40mL,相应的反应如下:
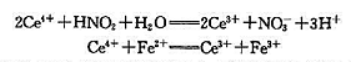
(1)若将第一个反应式作为原电池的电池反应写出该原电池的电极反应并计算该电池反应的ΔrGmθ[已知ϕθ(Ce4++/Ce3+)=1.44V,ϕθ(NO3-/NO2-)=0.934V]
(2)计算试样中NaNO2的质量分数w.[已知M(NaNO2)=69.00g.mol-1]
(3)计算第一步的标准平衡常数Kθ.
解题思路:注意原电池的写法.此题依然是考查电化与热力学、化学平衢间的计算.