 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知有A溶液浓度为14.65%NaCl溶液,又有B溶液浓度为0.75%的NaCl稀溶液,而工作需要浓度为3.50%,问利用上述二种溶液配制5000ml,浓度为3.50的工作溶液时各需AB多少ml?(用交叉法计算)。
暂无答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知有A溶液浓度为14.65%NaCl溶液,又有B溶液浓度为…”相关的问题
更多“已知有A溶液浓度为14.65%NaCl溶液,又有B溶液浓度为…”相关的问题
A、体积质量百分浓度;
B、质量百分浓度;
A.在溶液中加入一定量的KNO3溶液,难溶电解质溶解度增加
B.当某条件下IP=Ksp时,表示溶液是饱和的,沉淀和溶解达到动态平衡
C.在溶液中加入少量的NaCl溶液,可使溶解度减少
D.根据溶度积规则,沉淀生成条件是IP>Ksp
E.一定温度下,对于不同类型的难溶电解质来说,Ksp越大,溶解度越大
F.难溶性电解质在水溶液中都无法解离G、AgCl水溶液的导电性很弱,所以AgCl为弱电解质
(2007年)难溶电解质AgCl在浓度为0.01mol/L的下列溶液中,溶解度最小的是()。
A.NH3
B.NaCl
C.H2O
D.Na2S2O3
已知微溶化合物Ag2CrO3的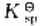 =1.12×10-12,Ag2CrO3,在0.01mol·L-1K2CrO4溶液中的溶解度为s1:在0.01mol·L-1AgNO3溶液中的溶解度为s2, 两者关系为()
=1.12×10-12,Ag2CrO3,在0.01mol·L-1K2CrO4溶液中的溶解度为s1:在0.01mol·L-1AgNO3溶液中的溶解度为s2, 两者关系为()
A.s1<s2
B.s1>s2
C.s1=s2
D.不确定
今有0.10mol.L-1Na2B4O7。溶液500mL,(1) 求溶液的pH(不考虑离子强度的影响):欲用上述溶液分别配制(2)pH=9.00,(3)pH=10.00的缓冲溶液。问各应加入什么溶液?各应加入多少毫升(设其浓度为2.0mol.L-1)?已知H3BO3的pK=9.24。