 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某含氧酸的化学式为HaMOb,其水溶液与氢氧化钡溶液恰好完全反应时两者的物质的量之比为1:1,则a的值为()
A.1
B.2
C.3
D.4
 答案
答案
B、2
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.1
B.2
C.3
D.4
 答案
答案
B、2
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某含氧酸的化学式为HaMOb,其水溶液与氢氧化钡溶液恰好完全…”相关的问题
更多“某含氧酸的化学式为HaMOb,其水溶液与氢氧化钡溶液恰好完全…”相关的问题
A.其单质都能与水反应,通式为X2+H2O═HX+HXO
B.HX易溶于水,其水溶液都是强酸
C.其单质都有颜色,都有毒
D.最高价含氧酸的通式为HXO4
A.X的氢化物稳定性强于W氢化物的稳定性
B.X的含氧酸比W的含氧酸酸性强
C.若X与Y原子序数相差5,则形成的化学式为Y2X3
D.简单离子半径X>Y>Z>W
A.用甲醛水溶液浸泡鱼虾,防止其变质
B.蔗糖的化学式为,它是食品中常用的甜味剂
C.缺乏维生素A会引起坏血病,缺乏维生素C会引起夜盲症
D.钙是人体内含量最高的金属元素,缺钙会导致骨质疏松、患佝偻病
A.有可能产生两种沉淀
B.不可能立即出现沉淀
C.不可能只有一种沉淀
D.有可能变为澄清溶液
推理判断:
(1)无色晶体(A)易溶于水,向其水溶液中滴加氯水,溶液变黄有(B)生成:继续滴加氯水时,黄色消失有(C)生成。向(A)的水溶液中滴加高氯酸生成白色难溶物(D)。向(B)的水溶液中滴加二氯化铁时有(E)生成,(E)与硫氰化钾溶液作用,有红色物质生成。向(C)的水溶液中加入(A),酸化后有(B)生成。
试给出(A),(B),(C),(D)和(E)的化学式,并完成各步反应的离子反应式。
(2)白色粉末是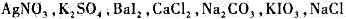 中某两种的混合物。该粉末加到水中形成白色沉淀,再加入稀硝酸酸化时白色沉淀消失且溶液发黄,再将溶液微热一段时间后滴加氨水至碱性,又形成白色沉淀且溶液变清。
中某两种的混合物。该粉末加到水中形成白色沉淀,再加入稀硝酸酸化时白色沉淀消失且溶液发黄,再将溶液微热一段时间后滴加氨水至碱性,又形成白色沉淀且溶液变清。
试判断原白色粉末的组成,说明理由并写出相关反应的方程式。
A.金属氧化物、氧化钠、Na2O2
B.酸性氧化物、二氧化硫、SO2
C.含氧酸、硫酸、H2SO4
D.正盐、纯碱、Na2CO3
A.元素X的氢化物比其他三种元素的氢化物都稳定
B.元素Y在自然界中只以化合态形式存在
C.元素Z的含氧酸只有两种
D.元素W、Y位于周期表中金属与非金属分界线附近
A.(1)发酵粉的主要成分为 (填化学式)
B.(2)下列物质的水溶液与发酵粉溶液酸碱性相同的是 (填序号)
C.①雕牌肥皂 ②威猛先生洁厕剂 ③百事可乐
D.(3)测得卡夫果珍的pH=5,将其和发酵粉混合后,放入水中产生的气体是
E.(填化学式)