 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在下列关于AL(OH)的描述中,不正确的是()
A.与四环素类药物合用,不影响其疗效
B.抗酸作用较强,奏效较慢
C.口服后产生氯化铝,有收敛、止血作用
D.久用可引起便秘
E.与三硅酸镁合用,可增加疗效
 答案
答案
A、与四环素类药物合用,不影响其疗效
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.与四环素类药物合用,不影响其疗效
B.抗酸作用较强,奏效较慢
C.口服后产生氯化铝,有收敛、止血作用
D.久用可引起便秘
E.与三硅酸镁合用,可增加疗效
 答案
答案
A、与四环素类药物合用,不影响其疗效
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在下列关于AL(OH)的描述中,不正确的是()”相关的问题
更多“在下列关于AL(OH)的描述中,不正确的是()”相关的问题
A.是银白色较软的金属
B.Tl(OH)3与Al(OH)3相似,也是两性氢氧化物
C.可以形成氧化物Tl2O3
D.与酸反应比铝剧烈
A.热稳定性:SiH4<H2S<H2O
B.酸性:HClO3>H2SO4>H3PO4
C.碱性:NaOH>Mg(OH)2>Al(OH)3
D.金属性:Na>Mg>Al
A.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
B.Na2O2应保存于密封、干燥带玻璃塞的广口瓶中
C.MgO的熔点很高,可用于制作耐高温材料
D.电解MgCl2饱和溶液,可制得金属镁
A.阳极反应为Fe-2e-===Fe2+
B.电解过程中溶液pH不会变化
C.过程中有Fe(OH)3沉淀生成
D.电路中每转移12 mol电子,最多有1 mol Cr2Oeq \o\al(2-,7)被还原
A.原子半径:Na<Mg<Al
B.热稳定性:HCl>H2S>PH3
C.酸性强弱:H2SiO3<H3PO4<H2SO4
D.碱性强弱:NaOH>Mg(OH)2>Al(OH)3
A.酸性:HClO4>HBrO4>HIO4
B.碱性:NaOH>Mg(OH)2>Al(OH)3
C.稳定性:PH3>H2S>HCl
D.非金属性:F>O>S
生产上用过量烧碱溶液处理某矿物(含Al2O3、MgO),过滤后得到的滤液用NaHCO3溶液处理,测得溶液pH、n[Al(OH)3]随加入NaHCO3溶液体积变化的曲线如下图所示。下列有关说法不正确的是()。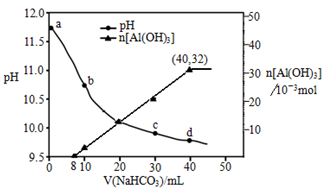
A.生成沉淀的离子方程式为HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-
B.b点与c点溶液所含微粒种类相同
C.a点溶液中大量存在的离子是Na+、AlO2-、OH-
D.NaHCO3溶液的物质的量浓度为0.8mol/L
A.氢气球遇火燃烧爆炸,因为氢气受热分子间间隙增大
B.人们食用豆浆,因其含有重要的营养物质蛋白质
C.制作馒头不能用吊白块来增白,因其会产生对人体的有害的物质
D.人胃酸过多可服用含Al(OH)3的药品,因其可中和过多胃酸
A.加热蒸干Na2CO3溶液,最后可以得到NaOH和Na2CO3的混合固体
B.除去MgCl2中的Fe3+,可以加入NaOH固体
C.明矾净水的反应:Al3++3H2O Al(OH)3+3H+
D.加热蒸干KCl溶液,最后得到KOH固体(不考虑CO2的反应)
A.l(OH)3 是难溶于水的白色沉淀
B.l(OH)3 能吸附水中的悬浮物
C.l(OH)3 能溶于氨水
D.l(OH)3属于两性氢氧化物
A.溶液X中一定含有H+、Al3+、NH+4、Fe2+、SO2-4
B.根据上述连续实验不能确定溶液X中是否含有Fe3+、Cl-
C.沉淀H为Al(OH)3、BaCO3的混合物
D.若X为100 mL,产生的气体A为44.8 mL(标况),则X中c(Fe2+)=0.06 mol•L-1